 |
| |||||||||||||||||||
|
La prevalenza dell�ipoacusia grave-profonda
di origine genetica o congenita nella popolazione neonatale sana ed in quella a
rischio audiologico e le conseguenti difficolt� psico-linguistiche e
relazionali del bambino, fonti di disagio individuale e sociale, inducono gli
Autori ad impostare un protocollo di screening audiologico neonatale con
l�intento di ottimizzarne l�esperibilit� nell�applicazione di un programma di
massa. A tale scopo si sono avvalsi della registrazione delle TEOAE, che sono
l�espressione di integrit� anatomo-funzionale della coclea, che ha acquisito
ormai, con unanime consenso, rilevanza non secondaria come test di screening
audiologico neonatale. In questo studio lo scopo � stato quello di
valutare la validit� della metodica con otoemissioni acustiche in uno screening
di massa, che viene tuttora eseguito dal Servizio di Audiologia dell�Ospedale
di Mantova su tutti i nuovi nati, con l�obiettivo di verificare la specificit�
del sistema e di ridurre al minimo il numero dei falsi allarmi senza inficiarne
l�attendibilit�. Ci� presuppone la sensibilizzazione e la collaborazione dei
genitori senza che ci� comporti una condizione di eccessiva ansiet�. Introduzione La sordit� nel bambino � sempre un problema grave e complesso. E�
necessaria una diagnosi molto precoce, possibilmente entro il 5� mese di vita,
per poter prendere tempestivamente tutti quei provvedimenti terapeutici e
riabilitativi di volta in volta necessari. E� stato calcolato con sufficiente approssimazione (ISTAT - 1992) che in
Italia circa 5.000.000 di persone presentano turbe uditive, fra queste, circa
70.000 sono considerate �sordomute� o, meglio, �sorde non rieducate�, nel senso
che presentano sordit� profonda sin dalla nascita e conseguenti notevoli
alterazioni nella formazione e nella maturazione del linguaggio, unitamente a
un grave impedimento nella comunicazione verbale. Oltre 600.000 soggetti,
inoltre, presentano gravi o gravissime turbe dell�udito che portano a grandi
difficolt� nell�inserimento scolastico e in seguito nel mondo del lavoro (1). Nonostante la frequenza delle ipoacusie permanenti nella popolazione
infantile risulti relativamente scarsa, a livello mondiale � auspicabile un
progetto comune di prevenzione sanitaria mirata ad una diagnosi precoce del
danno uditivo e delle sue conseguenze, dati gli effetti devastanti che questo
produce sullo sviluppo psicofisico degli individui affetti. Molto sinteticamente, si pu� affermare che l�assenza o la carenza grave
di informazione acustica induce nel bambino: mancata o insufficiente
acquisizione del linguaggio, disturbi comportamentali e del carattere,
alterazioni dello sviluppo psicomotorio, disturbi della percezione della sfera
spazio-temporale (2). L�American Academy� of Paediatrics (1999) sancisce la necessit�
di identificare le ipoacusie entro il terzo e non oltre il sesto mese di vita
per poter garantire la piena possibilit� di recupero delle abilit� uditive,
poich� si � dimostrato che quanto pi� precocemente viene ripristinata una
normale stimolazione acustica, tanto inferiore risulta in seguito il gap fra
bambino ipoacusico e bambino normoudente in termini di performance
comunicative, linguistiche, relazionali e cognitive. La riabilitazione pu� essere rapida
e pressoch� completa se, a una diagnosi precoce, segue l�immediato trattamento
protesico e riabilitativo, che oggi si avvale di due strumenti fondamentali,
vale a dire la protesi acustica e l�impianto cocleare, entrambi supportati da
un adeguato training logopedico (3). La protesizzazione acustica
dev�essere immediata anche nel caso in cui la precisazione del deficit sia in
dubbio. E� pi� dannosa l�assenza di stimolazione acustica nel periodo di
massima plasticit� linguistica che il pericolo di sovrastimolazione. Nel bambino piccolo che non abbia
iniziato a parlare la protesizzazione � senza utilit� se non viene affiancata
da una riabilitazione logopedica. Il logopedista, in base ai risultati
acquisiti, sar� in grado di confermare l�esatta impostazione di partenza o, in
caso contrario o dubbio, sollecitare una revisione diagnostica. I bambini sordi sottoposti a
riabilitazione entro il sesto mese di vita acquisiscono un linguaggio ed una
comunicazione verbale equivalente a quella di bambini normoacusici anche in
caso di ipoacusia severa e profonda. Da questi presupposti scaturisce la
necessit� di un test di screening universale infantile, inteso come un esame in
grado di identificare, in una popolazione ritenuta sana, un deficit non
evidente che possa causare un handicap o una disability significativa per la
quale esista la possibilit� di intervenire con un trattamento precoce ed
efficace. Lo screening non riguarda i casi di patologia sospetta da indagare
con una diversa procedura diagnostica. I metodi convenzionali di screening comportamentale
(reattometria) sono poco affidabili a causa dell�alto numero di falsi positivi
e dell�inaccettabile numero di falsi negativi. Il Boel test presenta un numero di falsi positivi
dell�1,5% se usato come test di screening. L�ABR soddisfa i criteri di affidabilit� in tutti i
casi, purtroppo il suo impiego, come metodica di screening, � penalizzato dal
tempo richiesto per la ricerca di soglia, che quindi ne limita l�utilizzo a
pochi soggetti selezionati ad alto rischio audiologico, e dal costo eccessivo
in virt� delle risorse umane impiegate. Al contrario le otoemissioni si sono rivelate di
facile applicazione, di basso costo e assolutamente prive di rischi per il
bambino, sono gi� evidenziabili in epoca precoce e facilmente registrabili
approfittando dei frequenti periodi di sonno caratteristici del neonato,
presentano, quindi, quelle caratteristiche di applicabilit� e di affidabilit�
che le rendono estensibili a livello universale (4). Otoemissioni acustiche come test di screening Uno dei capitoli pi� affascinanti della moderna audiologia � stato
aperto da David T. Kemp nel 1978 con la registrazione di suoni emessi
attivamente dalla coclea umana in seguito a una stimolazione sonora. Questi suoni, chiamati otoemissioni acustiche, si presentano con
un�intensit� particolarmente bassa e richiedono perci� tecniche particolari per
la loro evidenziazione (5). Nonostante alcune incertezze riguardo ai meccanismi fisiologici e al
tipo di strutture cocleari coinvolte, � unanimemente accettato che le otoemissioni
sono generate dalla attivit� contrattile delle cellule ciliate esterne
dell�organo di Corti e dalle caratteristiche meccano-strutturali della membrana
basilare con trasformazione di energia meccanica in energia acustica. Le otoemissioni acustiche sono presenti sia spontaneamente (otoemissioni
acustiche spontanee � SOAE) sia in seguito ad una stimolazione sonora
(otoemissioni acustiche evocate - EOAE) e possono essere registrate con un
adatto microfono posto nel condotto uditivo esterno, dopo che hanno attraversato
a ritroso le strutture cocleari, la catena ossiculare e la membrana timpanica
(6). Le otoemissioni acustiche evocate
sono classificate in base alle caratteristiche dello stimolo acustico
somministrato; quelle pi� comunemente utilizzate negli screening neonatali sono
le otoemissioni acustiche evocate transitorie (TEOAE), ottenute con click o con
tone-burst (7).� Nel 1988 fu sviluppata, presso i laboratori del �Institute of
Laryngology and Otology� di Londra, la prima apparecchiatura di registrazione
delle TEOAE sufficientemente semplice, miniaturizzata ed economica, tale da
poter essere immessa nel commercio. Questo sistema fu denominato dal nome
dell�istituto e dell�anno in cui fu messo a punto �ILO 88�. Successivamente fu immesso sul mercato un nuovo sistema capace di
registrare vari tipi di otoemissioni acustiche e denominato �ILO 92�. Nei neonati normoudenti le TEOAE sono presenti dal 99,8 al 100% dei
casi, per questo � sufficiente rilevare la loro presenza per formulare la
diagnosi di normoacusia. La soglia di detezione delle TEOAE aumenta progressivamente con la
perdita uditiva e sono sempre assenti nei bambini a termine in caso di
ipoacusia superiore ai 25 dB (8). La probabilit� di non identificare mediante le otoemissioni un bambino
ipoacusico con deficit retrococleare, nella popolazione neonatale esente da
fattori di rischio audiologico, � di 1:100 (un falso negativo ogni 100 soggetti
ipoacusici significa uno ogni 100.000 soggetti esaminati in caso di una
prevalenza di uno per mille) (9). Con questo studio gli Autori si sono proposti di valutare i risultati
ottenuti nello screening audiologico mediante registrazione delle TEOAE.
L�intento � stato quello di studiare la validit� della metodica in uno
screening di massa, che � tuttora eseguito su tutti i nuovi nati, con
l�obiettivo di verificare la specificit� del sistema e di ridurre al minimo il
numero dei falsi allarmi senza inficiarne l�attendibilit�. Ci� presuppone la
sensibilizzazione e la collaborazione dei genitori senza che ci� comporti una
condizione di eccessiva ansiet�. Metodi e Protocolli usati a Mantova Presso il Servizio di Audiologia dell�U.O. di Otorinolaringoiatria
dell�Ospedale �Carlo Poma� di Mantova, da luglio 2000 a dicembre 2001, sono
stati sottoposti a screening audiologico, mediante TEOAE, 1998 neonati, che
rappresentano il 100% dei nuovi nati nei 18 mesi di osservazione. I soggetti
testati� comprendevano sia i nati a
termine, normopeso, con indice di Apgar superiore a 8 e privi di fattori di rischio
audiologico (1778 soggetti), sia i nati pretermine o con qualsiasi tipo di
patologia evidente alla nascita, ricoverati presso l�U.O. di Patologia
Neonatale (220 bambini). La registrazione delle TEOAE � stata eseguita con Echoport-Otodynanamics
ILO 288 Analyzer (Fig.1) secondo i parametri tecnici ormai accettati e
standardizzati (modalit� di Quickscreen) ed � stata condotta in condizioni di
sonno spontaneo, dopo il pasto.  Figura 1: Echoport-Otodynanamics ILO 288 Analyzer Nei bambini nati a termine ricoverati presso l�U.O. di Neonatologia,
l�esame � stato effettuato al secondo giorno di vita nei nati spontanei e al
quarto giorno nei nati da parto distocico (I step), tutti i test sono stati
eseguiti presso l�U.O. di Ostetricia e Ginecologia. Nei bambini ricoverati presso la Patologia Neonatale il I step dello
screening � avvenuto qualche giorno prima della dimissione, quando peso e
condizioni fisiche sono state ritenute equivalenti a quelle di un bambino nato
a termine, ed � sempre stato eseguito nei locali della terapia intensiva, con
possibilit� di vari controlli fino al giorno della dimissione (Fig.2).� 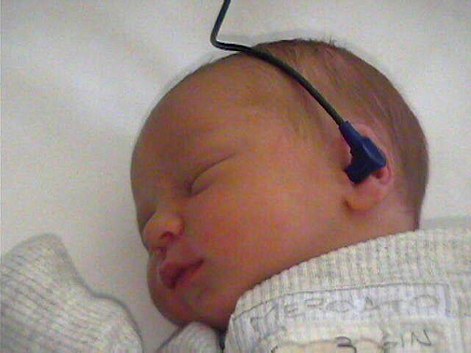 Figura 2: Un bambino nato a termine Se il bambino ha fallito il I step (�fail�), sia che si tratti di
neonati fisiologici che provenienti dalla Patologia Neonatale, si � eseguito un
test di controllo in coincidenza con la prima visita pediatrica, circa 20
giorni dopo la dimissione (II step), presso il Servizio di Audiologia (Fig.3). 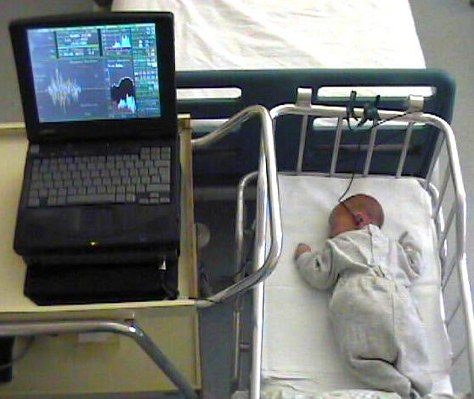 Figura 3: I �fail� persistenti alla seconda indagine, sono stati ricontrollati a
distanza di 20-40 giorni (III step a circa uno-due mesi di vita). In caso di
�fail� confermato, si � proceduto a: raccolta anamnestica, visita
otorinolaringoiatrica, esame impedenzometrico, test audiometrici
comportamentali (reattometria, Boel test) e infine ABR (Tab. 1).
���������
���������������������������� �����
� �������������������������������������������������������������������� Pass��������������� ����� ����� Fail
Tab. 1 � Protocollo di screening attraverso TEOAE Se il bambino non ha superato l�esame ABR � stato in seguito sottoposto
ad una ulteriore valutazione audiologica completa al fine di verificare
l�esistenza dell�ipoacusia, stabilirne il tipo e l�entit� ed iniziare il
programma di riabilitazione (10). Risultati Neonati fisiologici: dei 1778 neonati fisiologici 1689
(95%) sono �passati� al I step, con un totale di �fail� di 89 casi (5%), di cui
29 (32,6%) bilaterali e 60 (67,4%) monolaterali, con una prevalenza dei �fail�
monolaterali nell�orecchio sinistro (37 a sinistra vs 23 a destra).�
Di questi 89 bambini (37 femmine pari al 41,5%, e 52 maschi
corrispondenti al 58,5%) non si sono presentati al secondo controllo 8. Dei
rimanenti, 63 sono passati al II step, mentre in 18 casi persisteva almeno un
�fail� monolaterale. Al III step sono passati 6 bambini, 6 sono
risultati con �fail� persistente monolaterale, 5 con �fail� persistente
bilaterale e uno non si � presentato all�approfondimento diagnostico. Tutti i casi risultati �fail� al III step
sono stati sottoposti ad ABR: in 6 bambini l�esame era nella norma, in 3 ha
evidenziato un�ipoacusia di grado medio-lieve e nei restanti 2 un�ipoacusia di
grado medio-grave (un caso monolaterale e un caso bilaterale). Neonati patologici: dei 220 neonati ricoverati presso la
Patologia Neonatale 199 (90,5%) sono �passati� al I step, con un totale di
�fail� di 21 casi (9,5%), di cui 15 (71,4%) bilaterali� e 6 (28,6%) monolaterali (3 a destra e 3 a
sinistra). Di questi 21 bambini (5 femmine pari al 23,8%
e 16 maschi corrispondenti al 76,2%) non si sono presentati al secondo
controllo 3. Dei 18 bambini, 3 sono passati al II step, mentre in 15 casi
persisteva almeno un �fail� monolaterale. Al III step sono passati 4 bambini, 2 sono
risultati con �fail� persistente monolaterale, 7 con �fail� persistente
bilaterale e 2 non si sono presentati all�approfondimento diagnostico. Tutti i casi risultati �fail� al III step
sono stati sottoposti ad ABR: in 5 bambini l�esame era nella norma, in 1 ha
evidenziato un�ipoacusia di grado medio-lieve bilaterale e nei restanti 3
un�ipoacusia di grado grave bilaterale. Discussione Nei neonati fisiologici si � trovata
un�alterazione delle TEOAE nel 5% dei casi testati al I step, percentuale che �
scesa all�1% al II step e allo 0,6% al III step. Lo 0,2% dei neonati
fisiologici presentava un�alterazione del tracciato ABR (due casi di ipoacusia
neurosensoriale bilaterale medio-lieve, una ipoacusia neurosensoriale medio
grave bilaterale e una monolaterale). In un caso si � evidenziata un�ipoacusia
di tipo trasmissivo monolaterale (0,05%). Solo lo 0,5% dei bambini � sfuggito ai
controlli successivi al primo (8,9% dei �fail� al II step e 5,5% al III step). Nei neonati patologici si � trovata
un�alterazione delle TEOAE nel 9,5% dei casi testati al I step, percentuale che
� scesa al 6,8% al II step e al 4% al III step. Lo 0,9% dei neonati patologici
presentava un�alterazione del tracciato ABR (una ipoacusia neurosensoriale
bilaterale medio-lieve e una grave). In due casi si � evidenziata un�ipoacusia
di tipo trasmissivo bilaterale grave (0,9%). Il 2,2% dei bambini � sfuggito ai controlli
successivi al primo (14,2% dei �fail� al II step e 13,3% al III step). Se consideriamo la popolazione nel suo
insieme il nostro screening neonatale ha permesso l�individuazione precoce di 9
soggetti definibili come sordi pari a 0,5%. Questo dato risulta in accordo con
le percentuali di deficit uditivi neonatali riportate in letteratura,
considerando sia la popolazione a rischio (nati pretermine e/o con patologie
evidenti alla nascita) sia i neonati a termine senza evidenti fattori di
rischio audiologico (11,12,13). �������������� ������������������������������������������������������� Conclusioni Fra gli obiettivi sanitari occorrerebbe dare preminenza alla
diagnosi precoce e all�attuazione di misure preventive intese
all�identificazione universale di tutte le ipoacusie in grado di interferire
con un normale sviluppo del linguaggio. E� opportuno sottolineare come sia
vantaggioso avvalersi di metodiche obiettive in et� molto precoce sia per una
pronta identificazione delle turbe uditive, sia per la maggiore facilit� di
esecuzione degli esami condotti durante il sonno spontaneo del bambino
nell�epoca neonatale. I criteri che debbono guidare la scelta delle
metodiche impiegate per realizzare i depistage di massa della funzione uditiva
devono rispondere a particolari esigenze. Tali criteri comprendono: � l�accettabilit� � sia da parte del personale
che esegue lo screening, sia da parte della popolazione che lo subisce; � la semplicit� � impiego delle attrezzature
meno complesse e di costo pi� contenuto; � l�attendibilit� � stabilit� e ripetibilit�
dei risultati, verificate attraverso l�interosservazione, l�interprova e il
test-retest; � la validit� � percentuale di successo
diagnostico nei soggetti ipoacusici (14). Le otoemissioni si sono dimostrate un test affidabile che
consente di individuare in maniera oggettiva i soggetti con funzione uditiva
integra rispetto a quelli ipoacusici, con una facilit� e rapidit� di esecuzione
(cinque minuti circa) inusuali per le tecniche abitualmente utilizzate nella
diagnosi audiologica infantile e con un basso costo sia economico che di
risorse umane. I limiti di tale tecnica sono costituiti
dalla possibile, anche se rara, presenza di falsi positivi (talvolta difficolt�
tecniche di registrazione e/o caratteristiche fisio-anatomiche neonatali
inducono un�assenza parziale o totale delle otoemissioni) e dall�impossibilit�
di effettuare una diagnosi della sede e del tipo di ipoacusia eventualmente
riscontrata sulla base delle sole otoemissioni. Questo limite � facilmente
superabile indirizzando i casi dubbi verso indagini fondamentali per un
migliore inquadramento (ABR). Lo screening audiologico non � diventato
ancora routine a causa delle limitazioni tecnologiche e metodologiche
esistenti, di un diffuso atteggiamento attendistico da parte del medico e dei
genitori, della paura di incrinare il rapporto genitore/figlio notificando
l�anomalia del bambino, dell�ignoranza dell�epoca in cui � possibile effettuare
la diagnosi ed infine dei costi notevoli: lo screening non � mai semplice (15). Bibliografia 1.
Rollandi G.La
prevenzione e la diagnosi precoce. I disturbi dell�udito nel bambino. Milano:
Utet Periodici, 2000. 2.
Cavallazzi G.M.
La patologia uditiva in et� pediatrica. I disturbi dell�udito nel bambino.
Milano: Utet Periodici, 2000. 3.
De Caria A.R.
La protesizzazione acustica. I disturbi dell�udito nel bambino. Milano: Utet
Periodici, 2000. 4. Pelosi G., Hatzopoulos S., Chierici R., Vigi V.,
Martini A. Valutazione di un protocollo TEOAE lineare nello screening
audiologico neonatale: studio di fattibilit�. Acta Otorhinolaryngol Ital
18, 213-217,1998. 5. Bonfilis P. Avan P.
Distortion Product of Otoacoustic Emissions. Arch Otolaryngol Head and Neck
Surg 118, 1069-1076, 1992. 6.
Del Bo M.,
Giaccai F., Grisanti G. Manuale di Audiologia. Milano: Masson, 1995. 7.
Perez N.,
Fernandez S., Espinosa J.M. Distortion of otoacoustic emission. Acta
Otorrinolaringol Esp 44(4), 268-272, 1993. 8.
Martini A.,
Trevisi P. Prevenzione e screening dei deficit uditivi. I disturbi dell�udito
nel bambino. Milano: Utet Periodici, 2000. 9.
De Caria A.R.,
Monici M.M. Le otoemissioni acustiche. ORL Update. Milano: CRS Amplifon, 1999. 10.
White K.R., Vohr B.R., Beherens T.R. Universal newborn screening using
transient evoked otoacoustic emission: result of the Rhode Island Hearing
Assesment Project. Semin Hear,
14, 18-29, 1993. 11.
Molini E. Teoae
e screening audiologico neonatale. Le otoemissioni acustiche. Milano: CRS
Amplifon, 2000. 12. Kemp D.T. The past
and present status of hearing screening technology. ECSNHS edited by Grandori
& Lutman, 21-24, 1998. 13.
Pastrin G.,
Sergi P. Screening audiologico universale neonatale: esperienza presso la
Clinica Mangiagalli di Milano. Le otoemissioni acustiche. Milano: CRS Amplifon,
2000. 14. Quinonez R.E.
Crawford M.R. Longitudinal distortion-product otoacoustic emission latency
change in preterm neonates. Acta Otolaryngol (Stockh) 118, 26-31, 1998. 15.
Cianfrone G.
Limiti e vantaggi di un programma consorziato interospedaliero in Italia. Le
otoemissioni acustiche. Milano: CRS Amplifon, 2000. Data : Dicembre
2002 | |||||||||||||||||||
 |
 |

